Applikationswege in der Therapie der Multiplen Sklerose – monoklonale Antikörper im Fokus
4 PHARMAKOKINETIK, PHARMAKODYNAMIK UND SICHERHEIT MONOKLONALER ANTIKÖRPER IN DER MS-THERAPIE
4.4 SICHERHEITSASPEKTE
4.4.1 Pharmakodynamik der Lymphozyten-Depletion und -Repletion
Die Pharmakodynamik der Lymphozyten-Depletion sowie der -Repletion ist eine wichtige Kenngröße und Grundlage für die Wirksamkeit, aber auch die Sicherheit, der depletierenden monoklonalen Antikörper. So werden unter einer Alemtuzumab-Therapie die niedrigsten Lymphozytenwerte einen Monat nach der Behandlungsphase gemessen [EMA 2024]. Die Repletion der B-Zellen erfolgt innerhalb von sieben Monaten. Der Anstieg der T-Zellen ist hingegen langsamer, CD8+- und CD4+-T-Zellen überschreiten die untere Grenze der Norm (LLN) innerhalb von 20 bzw. 35 Monaten, die Ausgangswerte werden jedoch selten erreicht [Hill-Cawthorne et al. 2012]. Insgesamt weisen etwa 40 % der Patient*innen nach sechs Monaten eine gesamte Lymphozytenzahl ≥ LLN auf, nach zwölf Monaten ist dies bei ca. 80 % der Behandelten der Fall [Li et al. 2018]. Anzumerken ist, dass sich infolge einer Alemtuzumab-Therapie sekundäre Autoimmunphänomene, insbesondere Schilddrüsenerkrankungen und eine Immunthrombozytopenie, entwickeln können, denen eine B-Zell-Autoimmunität zugrunde liegt [Faissner und Gold 2018]. Auch Fälle von B-Zell-vermittelten sekundären ZNS-Erkrankungen wurden beschrieben [Haghikia et al. 2017]. Dies könnte im Zusammenhang mit einer Hyperrepopulation der B-Zellen nach drei bis sechs Monaten bei fehlender Regulation durch T-Zellen stehen [Baker et al. 2017b]. Aufgrund einiger Fälle von intrazerebralen Blutungen infolge der Anwendung von Alemtuzumab wurde 2019 durch die EMA eine Anwendungseinschränkung empfohlen [EMA 2019].
Wichtige Erkenntnisse zur Depletion und Repletion von B-Zellen durch Anti-CD20-Antikörper unter Berücksichtigung des Applikationswegs lieferten In-vivo-Daten aus Mausmodellen. So führte eine humanäquivalente, niedrig dosierte, subkutane Anti-CD20-Therapie zu einer schnellen Depletion (innerhalb von zwei Tagen) und Repletion (innerhalb von 21 Tagen auf 80 % des Ausgangswerts) von B-Zellen im Blut, in der Milz und in den Lymphknoten [Huck et al. 2019]. Dabei wurde im Vergleich zur intravenösen Applikation eine geringere Depletion von Marginalzonen-B-Gedächtniszellen und follikulären B-Zellen in sekundären Lymphorganen beobachtet, welche für eine schnelle und T-Zell-unabhängige antibakterielle Immunreaktion verantwortlich sind [Bigaud et al. 2023]. Im Vergleich zur intravenösen Anwendung wurden bei subkutaner Gabe auch geringere Antikörperkonzentrationen im Knochenmark festgestellt, sodass die dort aus den hämatopoetischen Stammzellen über CD20--pro-B-Zellen gebildeten CD20+-prä-B-Zellen besser erhalten blieben [Bigaud et al. 2022]. Der Erhalt der prä-B-Zellen ermöglicht eine schnellere Repopulation reifer naiver B-Zellen und erhöht damit die Flexibilität der Therapie.
Im Rahmen der klinischen Studien von Anti-CD20-Antikörpern zeigte sich unter Ocrelizumab eine vollständige Depletion der B-Zellen im Blut innerhalb von zwei Wochen [Hauser et al. 2017]. Die Repletion setzte sechs Monate nach der letzten Infusion ein und dauerte im Median 60 – 72 Wochen, sodass nach etwa 2,5 Jahren 90 % der Behandelten die LLN wieder überschritten hatten [Baker et al. 2020, Gibiansky et al. 2021]. Unter Ofatumumab wurde ebenfalls nach zwei Wochen bei 95 % der Patient*innen eine Reduktion der B-Zellen auf < LLN beobachtet und ab Woche 4 wiesen 92 % der Behandelten eine Zellzahl < 10/μl auf [Hauser et al. 2020a]. Die mediane Repletionsdauer nach dem Absetzen wird mit 24,6 Wochen angegeben und ist damit, wie anhand des Mausmodells vermutet, deutlich kürzer als bei den intravenös applizierten Anti-CD20-Antikörpern [EMA 2024]. Ublituximab führte in den Zulassungsstudien bereits 24 Stunden nach der ersten Injektion zu einer 96%igen Reduktion der medianen B-Zell-Zahlen, darüber hinaus blieb bis zum Studienende eine Reduktion um 97 % erhalten [Steinman et al. 2022]. Die mediane Repletionsdauer betrug 70 Wochen [EMA 2024].
4.4.2 Neutropenie
Während die Depletion von T- und/oder B-Zellen Grundlage des Wirkmechanismus der meisten Antikörperbasierten MS-Therapien ist, kann die Beseitigung weiterer Immunzelltypen mit zusätzlichen unerwünschten Effekten verbunden sein. Beispielsweise sind Neutropenien für die Sicherheit der depletierenden Antikörper von Interesse, da Neutrophile eine wichtige Komponente der frühen Immunantwort gegen Infektionen darstellen [Baker et al. 2024]. In Übereinstimmung mit der geringgradigen Expression von CD52 auf Neutrophilen wurden unter Alemtuzumab bei 20 – 25 % der Behandelten Neutropenien beobachtet [Baker et al. 2017a]. Diese waren meist mild bis mäßig ausgeprägt und traten überwiegend frühzeitig nach der Behandlung auf [Baker et al. 2017a, Gaitán et al. 2017]. Obwohl Neutrophile kein oder kaum CD20 exprimieren, wurden auch bei Anti-CD20-Antikörper-Therapien Neutropenien festgestellt. Unter der intravenösen Therapie mit Ocrelizumab und Ublituximab kam es bei 4,4 – 4,6 % bzw. 3,3 % der Studienteilnehmenden zu einer Reduktion der Neutrophilenzahl mit Grad ≥ 2 [Baker et al. 2024, Hauser et al. 2021]. Kennzeichnend für die Neutropenien war ein überwiegend spätes Auftreten mehr als vier Wochen nach der Behandlung [Hess et al. 2023, Pang et al. 2024, Rossi et al. 2022]. Die subkutane Gabe von Ofatumumab war über einen Studienzeitraum von vier Jahren mit einer Neutropenierate (Grad ≥ 2) von 0,6 % verbunden [Bar-Or et al. 2022]. Es gilt nun aufzuklären, welcher Mechanismus zur Reduktion der Neutrophilenzahlen durch Anti-CD20-Antikörper führt und welchen Einfluss der Applikationsweg hat.
4.4.3 Immunglobulin-Spiegel
Neben den positiven krankheitsmodifizierenden Effekten bei Menschen mit MS kann ein Eingriff in die B-Zell-Homöostase die Produktion von Antikörpern beeinträchtigen und somit unerwünschte Auswirkungen auf das Infektionsrisiko und die Impfantwort der Betroffenen haben. Im Allgemeinen wird daher beispielsweise empfohlen, den Impfstatus vor Beginn einer solchen Behandlung zu aktualisieren.
So wurde unter Alemtuzumab einerseits eine signifikante Reduktion der Serumspiegel von Immunglobulin G (IgG), IgM und IgA zwölf und 24 Monate nach Beginn der Behandlung beobachtet [Möhn et al. 2020], andererseits konnte eine annähernd normale bzw. nur leicht reduzierte Impfantwort auf verschiedene Impfstoffe, darunter Severe-Acute-Respiratory-Syndrome-Coronavirus-2-(SARS-CoV-2-)Impfungen, gezeigt werden [Bsteh et al. 2022, McCarthy et al. 2013].
Aufgrund des Wirkmechanismus ist Natalizumab nicht mit dem Risiko einer Lymphopenie verbunden, vielmehr kommt es zu einem Anstieg zirkulierender T- und B-Zellen in der Peripherie [Krajnc et al. 2022]. Dennoch wurde eine Reduktion der IgG- und IgM-Spiegel beobachtet, deren klinische Relevanz allerdings bislang unklar ist [Szepanowski et al. 2021], denn dessen ungeachtet wurde bei Betroffenen unter Natalizumab-Behandlung eine ausreichende Immunreaktion auf verschiedene Impfstoffe festgestellt [Bsteh et al. 2022, Kaufman et al. 2014].
Da die Antikörper-produzierenden Plasmazellen kein CD20 exprimieren, stellen sie kein direktes Angriffsziel der Anti-CD20-Antikörper dar. Weil ihre Entwicklung jedoch aus CD20+-Zellen erfolgt, kann eine Hypogammaglobulinämie aus der Langzeitanwendung der Anti-CD20-Antikörper resultieren. So führte Ocrelizumab an Woche 96 der zulassungsrelevanten Studien bei 1,5 %, 2,4 % und 16,5 % der Behandelten zu einer Senkung der IgG-, IgA- bzw. IgM-Spiegel auf < LLN und dieser Anteil stieg nach 5,5 Jahren auf 5,7 % (IgG), 5,4 % (IgA) und 29,2 % (IgM) [Derfuss et al. 2020, Hauser et al. 2017]. Die durchschnittliche Reduktion der Serumspiegel betrug zu diesem Zeitpunkt 17 % (IgG), 21,3 % (IgA) und 58,1 % (IgM) und die niedrigere IgG-Menge war mit einer erhöhten Rate schwerwiegender Infektionen assoziiert [Derfuss et al. 2020]. Personen, die mit Ocrelizumab behandelt wurden, zeigten eine vorhandene, aber abgeschwächte humorale Immunantwort auf verschiedene inaktivierte Impfstoffe [Bar-Or et al. 2020]. Im Falle einer SARSCoV-2-Impfung erwies sich die Antikörperproduktion als deutlich abgeschwächt, wohingegen die T-Zell-Antwort erhalten blieb [Räuber et al. 2022]. In einer kleinen Studie mit 43 Teilnehmenden bestätigten sich die Beobachtungen aus dem Mausmodell, dass bei der subkutanen Gabe von Ofatumumab gegenüber der intravenösen Ocrelizumab-Therapie ein größerer Anteil an B-Gedächtniszellen erhalten bleibt. Zudem waren die IgG-Spiegel im Vergleich zu gesunden Personen nur unter Ocrelizumab signifikant verringert, nicht unter Ofatumumab [Haase et al. 2023]. Auch in einer klinischen Langzeitstudie war Ofatumumab bis zu fünf Jahre mit einem stabilen Serum-IgG-Spiegel verbunden: 98 % der Behandelten hatten einen Wert > LLN. Zwar zeigte sich ein Rückgang der durchschnittlichen IgM-Spiegel, doch auch hier wiesen noch 69,4 % der Patient*innen einen Wert > LLN auf. Zudem zeigte sich keine Assoziation zwischen reduzierten Ig-Spiegeln und dem Risiko für schwerwiegende Infektionen [Cohen et al. 2023]. Die Impfantwort auf die SARSCoV-2-Immunisierung war in mehreren kleinen Studien dennoch durch eine schwächer ausgeprägte humorale Immunität, aber eine erhaltene zelluläre Immunantwort gekennzeichnet [Faissner et al. 2022, Ziemssen et al. 2022, Ziemssen et al. 2023]. Für das erst kürzlich zugelassene Ublituximab fehlen bislang Langzeitdaten sowie Daten zur Impfantwort. Der Anteil an Personen mit einem Serumspiegel < LLN lag in den Zulassungsstudien nach 96-wöchiger Behandlung bei 6,5 % (IgG), 2,4 % (IgA) und 20,9 % (IgM) [Steinman et al. 2022].
4.4.4 Infektionen
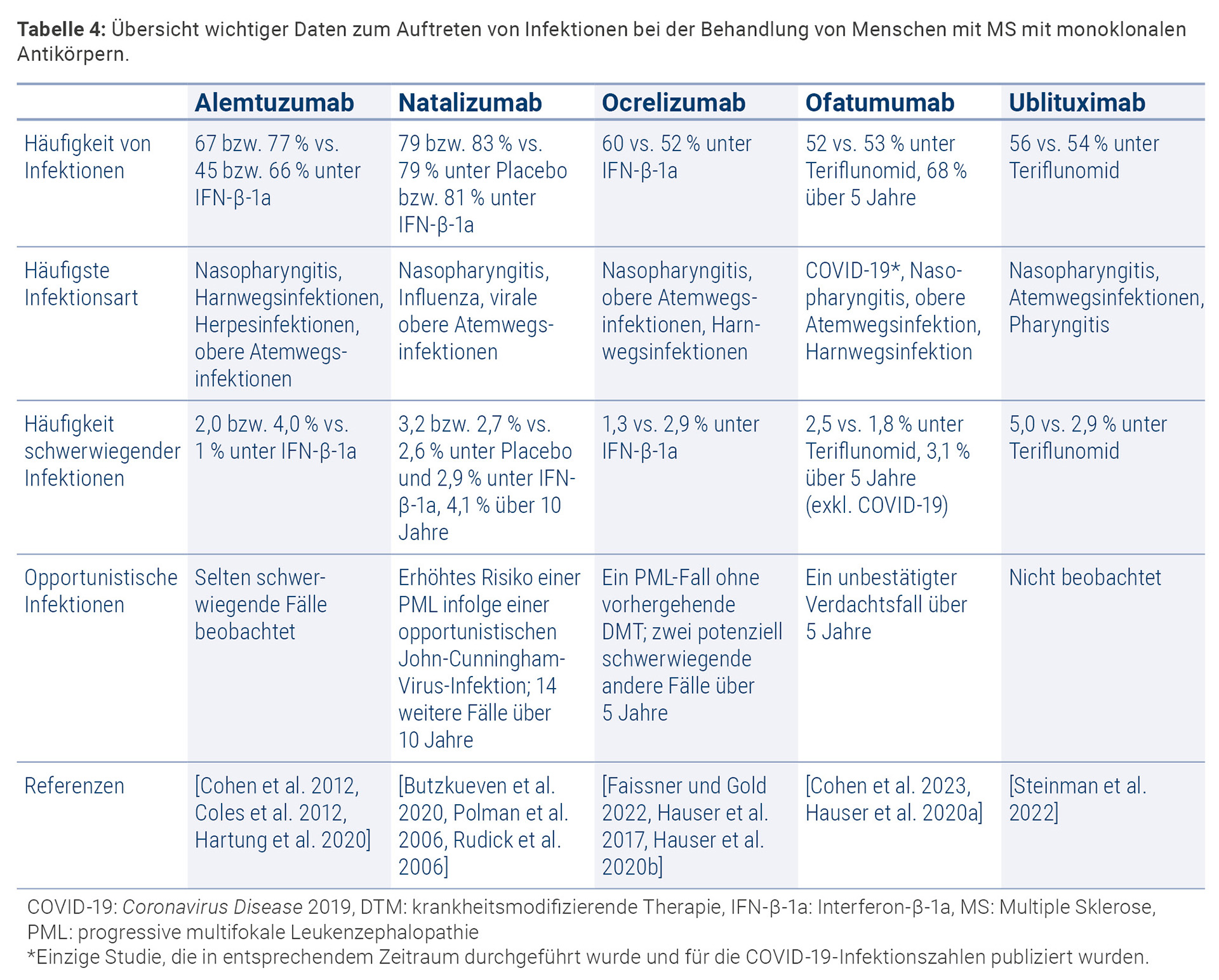
Wie bereits oben beschrieben, kann ein Eingriff in die Lymphozyten-Homöostase mit einem Risiko für Infektionen verbunden sein, sodass sich hieraus ein wichtiges Sicherheitsmerkmal der Antikörpertherapien ergibt. Tabelle 4 gibt daher eine Übersicht über die wichtigsten Daten zum Auftreten von Infektionen bei der Behandlung mit monoklonalen Antikörpern.
4.4.5 Infusions- und Injektions-bedingte Reaktionen
Infusions- oder Injektions-bedingte Reaktionen (IRR) werden durch eine Typ-2-Hypersensitivitätsreaktion mit Zytokinfreisetzung verursacht und treten während oder bis zu 24 Stunden nach einer Infusion bzw. Injektion auf. Um die Häufigkeit und Schwere von IRR zu reduzieren, kann bei intravenös verabreichten Antikörpertherapien eine Prämedikation mit Glukokortikoiden, Antipyretika (z. B. Paracetamol) und/oder Antihistaminika (z. B. Dimetinden) angezeigt sein. Darüber hinaus kann eine bis zu zweistündige Beobachtung der Behandelten im Anschluss an die Infusion erforderlich sein [EMA 2024].
Bei der Behandlung mit Alemtuzumab lag die IRR-Rate in den Phase-III-Studien bei ca. 90 % und etwa 3 % der Behandelten erlitten schwerwiegende IRR [Cohen et al. 2012, Coles et al. 2012]. Dabei waren die Reaktionen meist leicht bis mäßig ausgeprägt und traten beim ersten Behandlungszyklus häufiger auf als in den nachfolgenden Zyklen. Kopfschmerzen und Hautausschlag gehören zu den häufigsten IRR unter Alemtuzumab, es wurde jedoch auch von Fällen spontaner intrakranieller Blutung berichtet [Azevedo et al. 2019]. Infolgedessen wurde eine neue Risikobewertung durch die EMA durchgeführt und eine neue Risikostrategie formuliert [EMA 2022]. In den Zulassungsstudien von Natalizumab hatten 24 % der Behandelten eine IRR (am häufigsten Kopfschmerzen) bis zwei Stunden nach Infusionsbeginn im Vergleich zu 18 und 20 % unter Placebo bzw. IFN-β-1a [Polman et al. 2006, Rudick et al. 2006]. Unter Ocrelizumab betrug die IRR-Rate 34 % gegenüber 9,7 % in der IFN-β-1a-Kontrollgruppe, wobei 93 – 97 % der IRR in den Ocrelizumab-Gruppen von leichtem oder mäßigem Schwergrad waren. Die Reaktionen traten meist im Zusammenhang mit der ersten Infusion auf und Pruritus und Hautausschlag waren am häufigsten [Mayer et al. 2019]. Die subkutane Applikation von Ofatumumab war bei 20 % der Patient*innen mit einer systemischen IRR verbunden (99,9 % mit leichtem oder mäßigem Schweregrad), verglichen mit 15 % unter Placebo-Injektionen in der Teriflunomid-Kontrollgruppe [Hauser et al. 2020a]. In der Langzeitstudie über fünf Jahre lag der Anteil der Behandelten mit IRR bei 26 % [Cohen et al. 2023]. Die meisten systemischen Reaktionen traten bei der ersten Anwendung von Ofatumumab auf; Kopfschmerzen und Hitzewallungen waren am häufigsten [Hauser et al. 2020a]. In einer deutschen Real-World-Beobachtungsstudie berichteten die Patient*innen zwar initial häufiger von Schüttelfrost/Fieber und Kopfschmerzen (48 bzw. 46 %), doch bei den Folgeanwendungen gingen diese IRR in Übereinstimmung mit den klinischen Studien deutlich zurück [Klimas et al. 2023]. Ein ähnliches Bild zeigte sich für die Therapie mit Ublituximab: Hier betrug die IRR-Rate insgesamt 48 % im Vergleich zu 12 % unter Placebo, wobei bei der ersten Infusion 43 % der behandelten Personen eine IRR entwickelten. Bei 97 % der Betroffenen waren die Reaktionen leicht bis mäßig ausgeprägt; am häufigsten kam es zu Fieber [Fox et al. 2022, Steinman et al. 2022].